안녕하세요. 별구 입니다.
원료의약품 (변경)등록 및 연계심사 가이드라인(종전 완제의약품 중심 허가·심사 운영 관리 방안 관련 질의응답집) 자료가 공개 되었습니다.
이 문서는 ‘원료-완제의약품 연계심사’를 시행함에 따라 원료의약품 (변경)등록 업무를 포함하여 품질 평가 시 필요서류 및 변경관리 유형에 대하여 알기 쉽게 설명하거나 식품의약품안전처의 입장을 기술한 것입니다.
원료의약품 (변경)등록 및 연계심사 가이드라인(종전 완제의약품 중심 허가·심사 운영 관리 방안 관련 질의응답집) 자료는 '2025년 12월 26일' 자로 식품의약품안전처의 홈페이지에 게시 되었습니다.
그 내용은 다음과 같습니다.

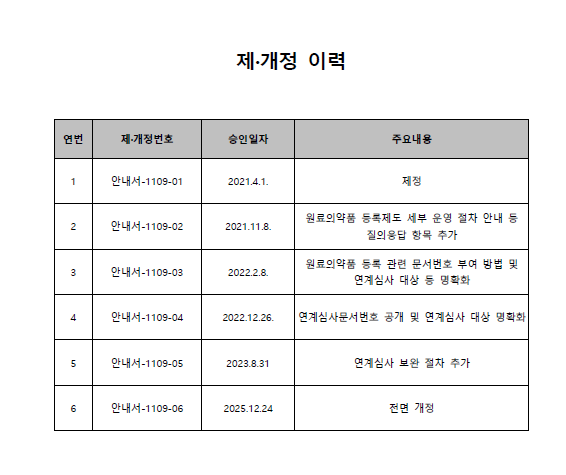
그 제개정은 다음과 같습니다.
목차는 다음과 같습니다.


자세한 사항은 첨부자료 확인 부탁드립니다.
원료의약품 (변경)등록 및 연계심사 관련 진행 시 참고자료로 활용하면 좋을 것 같습니다.
원료의약품+(변경)등록+및+연계심사+가이드라인+개정(최종).pdf
1.51MB
식품의약품안전처>법령/자료>법령정보>공무원지침서/민원인안내서>민원인안내서 - 상세보기 | 식품의약품안전처
반응형
'품질보증(QA) > 안내서_지침서 등' 카테고리의 다른 글
| 「2025 바이오의약품 산업동향 보고서」 (2025.12) 발간 안내 (0) | 2026.01.02 |
|---|---|
| 오염관리전략(CCS, Contamination Control Strategy) 작성 양식 배포 알림 (0) | 2026.01.02 |
| 2025년 식품의약품통계연보(제27호) (0) | 2025.12.31 |
| 2025년 의약품 허가특허연계제도 영향평가 결과보고서 (0) | 2025.12.31 |
| 디지털 기술이 적용된 기기를 활용한 임상시험 자료 수집 가이드라인 (0) | 2025.12.31 |