안녕하세요. 별구 입니다.
신생아 및 미숙아 대상 임상시험 가이드라인(민원인 안내서)가 공개 되었습니다.
이 안내서는 ‘신생아 및 미숙아를 대상으로 하는 임상시험 시 고려사항’에 대한 식품의약품안전처의 입장을 기술한 것입니다.
신생아 및 미숙아 대상 임상시험 가이드라인(민원인 안내서)은 '2024년 9월 30일' 자로 식품의약품안전처의 홈페이지에 게시 되었습니다.
식품의약품안전처>법령/자료>법령정보>공무원지침서/민원인안내서>민원인안내서 | 식품의약품
신생아 및 미숙아 대상 임상시험 가이드라인(민원인 안내서) '신생아 및 미숙아 대상 임상시험 가이드라인(민원인 안내서)' 개정을 알려드리니 업무에 참고하시기 바랍니다. 첨부파일 첨부파일
www.mfds.go.kr
개정이력은 다음과 같습니다.
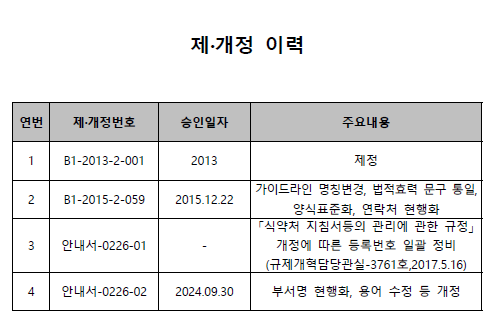
세부사항은 다음과 같습니다.
1. 서론
2. 신생아 및 미숙아를 대상으로 하는 임상시험
자세한 사항은 첨부자료 확인 부탁드립니다.
신생아 및 미숙아 대상 임상시험 시 진행할 때 참고자료로 활용하면 좋을 것 같습니다.
신생아+및+미숙아+대상+임상시험+가이드라인(민원인+안내서).pdf
0.37MB
반응형
'품질보증(QA) > 안내서_지침서 등' 카테고리의 다른 글
| 의약품 임상시험 계획(변경) 승인 보완사례집(민원인안내서) (0) | 2025.01.17 |
|---|---|
| 임상시험에서 유전체 시료수집 및 자료 관리 가이드라인(민원인 안내서) (0) | 2025.01.17 |
| 고령자 대상 임상시험 가이드라인(민원인 안내서) (0) | 2025.01.17 |
| 인체조직 기증이식 적합성 평가 가이드라인[민원인 안내서] (0) | 2025.01.17 |
| 의약품 소량포장단위 공급 관련 주요 질의응답 배포 안내 (0) | 2025.01.17 |